30/74
nã o u t i l i z e u m s i s t e m a d e m o n i t o R i z a ç ã o pRe s s i o ® e o c a t e t e R pR e s s i o ® i m p l a n t a d o ,
a o m e m o t e m p o q u e u m i n s t R u m e n t o e l e c t R o -c i R ú R g i c o d e a l t a f R e q u ê n c i a o u q u e
u m d e s f i b R i l h a d o R . se o f i z e R, p o d e d a n i f i c a R o c a t e t e R e/o u o s i s t e m a d e m o n i t o R i z a ç ã o
o u p e R t u R b a R o R e s p e c t i v o f u n c i o n a m e n t o .
Complicações / Efeitos secundários9.
As complicações que podem resultar da implantação de um sistema de monitorização
Pressio® incluem os riscos inerentes a qualquer intervenção cirúrgica e à inserção
de corpos estranhos.
Infecção
A principal complicação associada a este tipo de monitorização é a infecção.
Os riscos de infecção podem ser reduzidos utilizando técnicas de assepsia durante
o manuseamento e implantação do cateter e adoptando uma duração máxima da
implantação do cateter (5 dias). No caso de ser necessário continuar a monitorizar
após este período recomenda-se a colocação de outro sistema, noutro local.
Em caso de infecção, está indicada a remoção do sistema conjuntamente
com o início de tratamento especíco por via geral ou intratraqueal.
Hemorragia cerebral
Durante uma monitorização deste tipo, também pode ocorrer hemorragia cerebral.
A probabilidade de ocorrência desta complicação pode ser reduzida limitando o
número de incisões cerebrais durante o processo de introdução e assegurando que
este procedimento só é efectuado por prossionais treinados e competentes.
Estas complicações requerem a rápida intervenção de um médico.
Garantia10.
Os desempenhos do kit de monitorização Pressio® só são garantidos com a gama
de sistemas de monitorização Pressio® e com os acessórios concebidos, testados e
fabricados pela Sophysa.
A Sophysa garante que este dispositivo médico está isento de defeitos de material ou
de mão-de-obra. Para além desta garantia, a Sophysa não fornece qualquer outra
garantia, expressa ou implícita, incluindo a comercialização ou adaptação para um
uso especíco. A Sophysa não se responsabiliza por nenhum incidente, complicação,
lesão ou prejuízo resultante directa ou indirectamente do uso deste dispositivo. A
Sophysa não autoriza ninguém a assumir, em seu nome, responsabilidade pelos seus
produtos.
Processamento dos produtos após a 11.
utilização
Destruição após a utilização
Um dispositivo Pressio® desembalado, usado ou explantado tem de ser destruído em
conformidade com os procedimentos adoptados na instituição médica.
Devolução de produtos
Caso seja necessário devolver um kit de monitorização Pressio® explantado à Sophysa,
é necessário indicar se o mesmo foi submetido a limpeza.
Para avaliar convenientemente o produto devolvido, é necessário juntar-lhe um
formulário de Autorização de Devolução ao Fabricante.
No t a s :
p
a R a u m a a n á l i s e m a i s e f i c i e n t e , R e c o m e n d a -s e q u e n ã o l i m p e o d i s po s it i v o .
n
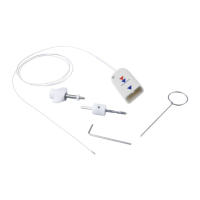
o c a s o d e u m k i t pR e s s i o ®, p a R a p a R ê n q u i m a , c o m p a R a f u s o , R e t i R e o c a t e t e R d o p a R a f u s o
c o m c u i d a d o .
Símbolos12.
Referência do catálogo
Fabricante
Método de esterilização pelo Óxido de Etileno
Não reutilizar
Não voltar a esterilizar
Data de validade
Código de lote
Número de série
Marcação de Conformidade CE
Consulte as Instruções de Utilização
EQUIPAMENTO DO TIPO BF: Conferindo um
grau adequado de protecção contra o choque
eléctrico, possuindo uma secção aplicada isolada
do Tipo F (utuante).
Condições de temperatura para armazenamento
e transporte
Guardar em local seco
Frágil, manuseie com cuidado
 Loading...
Loading...